Innovatieve nanotransistor voor eenvoudige meting elektrolytengehalte in bloed
Een bloedonderzoek bij patiënten waarvan de arts vermoedt dat ze lijden aan een probleem met de elektrolytenbalans vergt meestal veel inspanning doordat diverse selectieve testen uitgevoerd dienen te worden. Elektrolyten zijn bepaalde voedingsstoffen of chemicaliën in het lichaam die tal van belangrijke functies hebben zoals het regelen van de hartslag. Een verstoring van de elektrolytenbalans kan gevaarlijk zijn. Vanuit de chemie wordt gekeken naar de chemische verbindingen van elektrolyten, deze zijn gedeeltelijk in ionen gesplitst en geleiden elektrische stroom. Remco Hartkamp, universitair docent computational chemical physics bij de afdeling Process & Energy, ontwikkelde samen met onderzoekers van het Centre National de la Recherche Scientifique (CNRS) in Frankrijk en de NTT Basic Research Laboratories in Japan een nieuwe methode om de concentratie van diverse elektrolyten in het lichaam op een eenvoudigere manier te kunnen meten door het gebruik van een nanotransistor. De resultaten van het onderzoek ‘Selective layer-free blood serum ionogram based on ion-specific interactions with a nanotransistor’ zijn gepubliceerd in het mei-nummer van Nature Materials.

Samenvatting ‘Selective layer-free blood serum ionogram based on ion-specific interactions with a nanotransistor’
(alleen in het Engels beschikbaar)
The researchers presented what they called a ‘0D’ ion-selective field-effect transistor (ISFET), with a sensor of just 25 nm - much smaller than the conventional nanowire ISFETs. Compared to currently available devices, the 0D-ISFET showed a qualitatively different response to changes in pH and a much higher sensitivity to the presence of electrolytes, making it possible to sense electrolytes that are present in very small concentrations. Combining the experiments with molecular dynamics simulations and site-binding theory, new insight was acquired. Specifically, a theoretical approach to the trends found in the experimental measurements suggested an additive, rather than competitive, effect of mixed electrolytes on the electric potential at the solid-liquid interface. Furthermore, simulations suggested that the high sensitivity of the 0D-ISFET, especially with respect to divalent ions, may be caused by an excess of cations adsorbing onto the charged solid surface. Such overscreening is ascribed to a combination of electrostatic correlations and ion-specific adsorption.
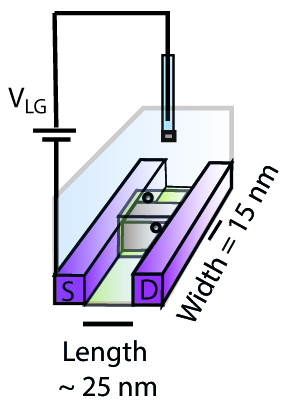
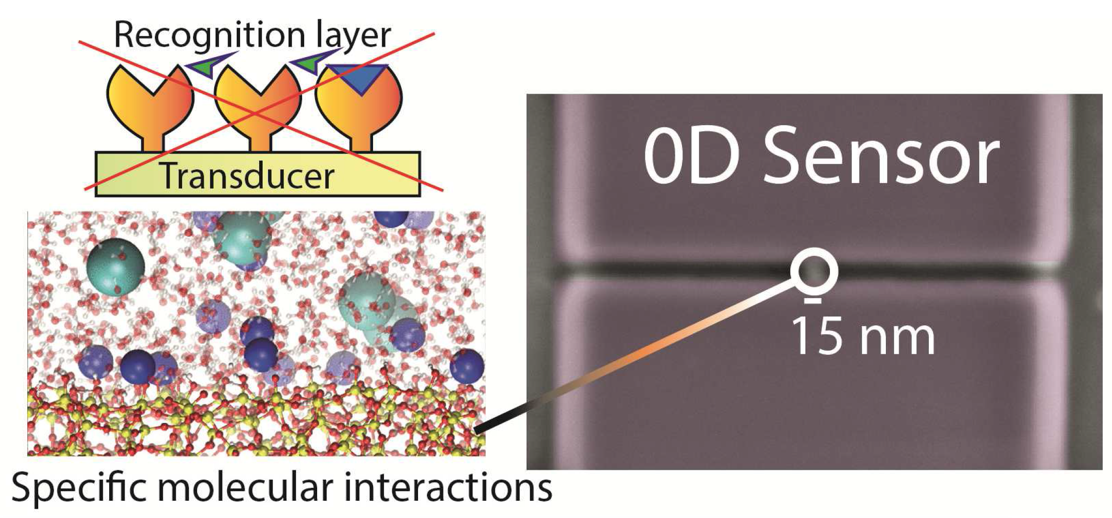
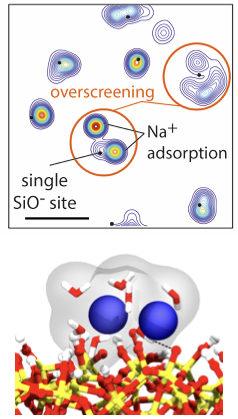
The 0D-ISFET can facilitate much cheaper and easier bedside testing, with only a tiny amount of blood needed. These developments are particularly important for patients who undergo regular ionogram measurements (for hyperkalemy or renal insufficiency) or who take antidiabetic, corticoid or lithium medications. Apart from the envisioned application in blood analysis, gaining an improved molecular-level understanding of ion specificity at the solid-electrolyte interface is important to a plethora of other applications. The marriage between experiments, simulations and theory is pivotal in the quest for gaining this molecular-level insight. The present collaborative study has taken important steps towards more accurate and versatile blood analysis at low cost and has improved fundamental understanding of ion-specific adsorption. Regardless, much more is to be learned both on the fundamental and applied side and further study is being performed to complement the present data and build on the current findings.
Lees meer over Remco Hartkamp