Nieuw Cas9-model brengt knipgedrag van DNA voor het eerst in kaart
Onderzoekers van de TU Delft hebben een natuurkundig model ontwikkeld dat een kwantitatief kader schetst over hoe gen-editing met CRISPR-Cas9 werkt, en dat hen in staat stelt te voorspellen waar, met welke waarschijnlijkheid, en waarom fouten in targeting (off-targets) optreden. Dit onderzoek, dat is gepubliceerd in Nature Communications, geeft ons voor het eerst een gedetailleerd fysisch inzicht in het mechanisme achter het belangrijkste gen-editing platform van vandaag.
De ontdekking van het CRISPR-Cas9 eiwit heeft gen-editing sterk vereenvoudigd. Dit wekte de hoop dat er een remedie kan worden gevonden voor veel erfelijke ziekten. Echter, om deze techniek veel en veilig in te kunnen zetten bij de behandeling van mensen, vereist dit uiterste precisie en voorspelbaarheid van de eventuele off-target effecten. Het onderzoeksteam van Martin Depken van de afdeling Bionanoscience bij de TU Delft toont nu een nieuw, natuurkundig model dat de bestaande modellen sterk verbetert: het model voorspelt niet alleen waar het DNA waarschijnlijk zal worden geknipt, maar ook met welke kans dat gebeurt.
Natuurkundige benadering om Cas9-gen-editing te begrijpen
Een grote beperking van de huidige bio-informatica modellen voor gen-editing, is dat ze binair van aard zijn: ze classificeren het knippen van targets op het genoom als waarschijnlijk of onwaarschijnlijk. Deze modellen richten zich alleen op targeting-fouten (off-targets) met een zeer hoge waarschijnlijkheid, en missen de lagere kans van vele off-targets die gezamenlijk toch de meerderheid van de editing-fouten in het genoom zouden kunnen vormen. Het nieuwe natuurkundig model van de onderzoekers houdt rekening met zowel kansrijke off-targets als kansarme off-targets; het model kan worden gebruikt om elke Cas9-variant natuurkundig te karakteriseren en voorspelt voor elk stuk op het genoom de kans dat die wordt geknipt.
Martin Depken legt de nieuwe natuurkundige aanpak van zijn lab uit: "Bij gen-editing wil je de waarschijnlijkheid van knippen op de beoogde plaats maximaliseren, terwijl je de kans minimaal wilt maken dat er in de rest van het genoom wordt geknipt. Het is daarom cruciaal om het knippen te kunnen begrijpen in termen van waarschijnlijkheden. Op basis van experimenten in de single-molecule physics en structurele gegevens kwamen we tot een model dat dit kan doen. We hebben de manier waarop gen-editing wordt omschreven, veranderd van een binaire keuze naar een volledig beeld op basis van kansen."
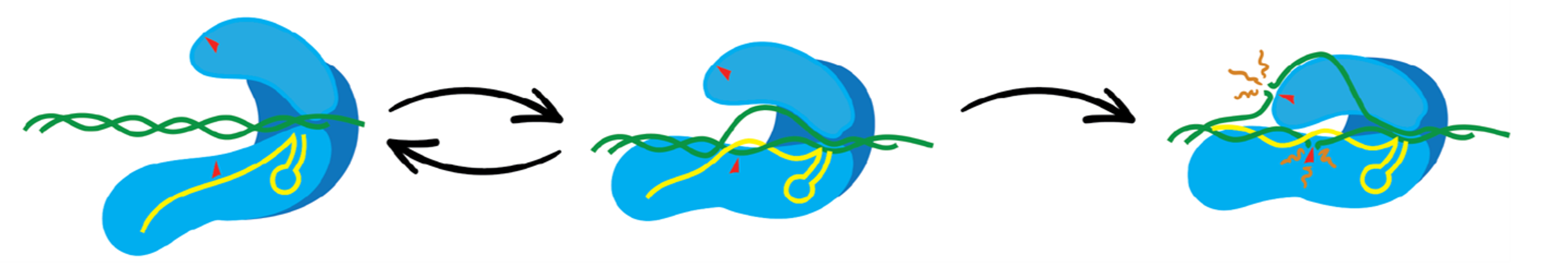
Precisie van gen-editing verbeteren
Omdat dit onderzoek natuurkundig inzicht geeft in waarom off-targets (fouten) optreden, markeert dit onderzoek ook een belangrijke volgende stap naar een meer rationele manier van ontwerpen van editing platforms, en van het karakteriseren, evalueren en vergelijken van bestaande platforms. De onderzoekers hopen met hun kansenbenadering van gen-editing ook bij te dragen aan een betere risico inschatting van genoom editing, doordat het model rekening houdt met alle mogelijke off-targets.
"Samen met onze experimentele samenwerkingspartners van de University of Texas in Austin hebben we met ons model Cas9 nu gebenchmarkt," zegt Depken. "Ons volgende doel is om hetzelfde te doen met andere nauwkeurige platforms voor gen-editing, om te begrijpen hoe en waarom ze verschillen. Hiermee hopen we het pad vrij te maken naar meer nauwkeurigheid in gen-editing.”
