Onderzoekers ontdekken hoe het pantser van een cel zowel flexibel als sterk kan zijn
Middeleeuwse ridders hadden ofwel een dik, log harnas, of ze konden een minder beschermend harnas dragen en flexibel zijn in de strijd - ze konden niet allebei hebben. Maar cellen kunnen dat wel. Onderzoekers van de TU Delft, de Universiteit van Leeds, het Institut Fresnel in Marseille en het Institut Curie in Parijs ontdekten dat eiwitten die 'septines' worden genoemd het kwetsbare membraan van een cel versterken, terwijl ze toch flexibel genoeg zijn om de cel in staat te stellen van vorm te veranderen.
Cellen zijn de bouwstenen van het leven. Zij kunnen als onafhankelijke eenheden optreden door gebruik te maken van een beschermend omhulsel, dat de uitwisseling van moleculen met hun omgeving strak regelt. Dit omhulsel moet zo zacht en vervormbaar zijn dat de cel van vorm kan veranderen, maar ook zo sterk dat het externe krachten kan weerstaan. Cellen lossen dit op door een zacht en fragiel membraan van fosfolipiden te koppelen aan het zogenaamde cytoskelet. Dit is een structuur van eiwitten die aan het membraan verankerde vezelnetwerkem vormen. De bekendste eiwitstructuur die bijdraagt aan het ‘pantser’ van de cel is het actinecytoskelet. Recent onderzoek wijst er echter op dat hierbij mogelijk een tweede soort eiwit betrokken is, namelijk septines.
Nieuwe netwerken
Om te begrijpen of en hoe septines het celmembraan versterken, bouwde een internationaal team van onderzoekers onder leiding van Gijsje Koenderink van de TU Delft synthetische celmodellen die het celmembraan in een geïsoleerde omgeving nabootsen. De onderzoekers zuiverden septines uit fruitvliegjes en bestudeerden met behulp van krachtige microscopiemethoden de structuren die door septines worden gevormd op modelfosfolipidemembranen. “We ontdekten dat septines dichte maar dunne netwerken vormen van dicht opeengepakte clusters filamenten, die mechanisch rigide zijn en daarom ideaal voor de versterking van een membraan”, zegt promovendus Gerard Castro-Linares van de TU Delft.
Gestructureerde linten
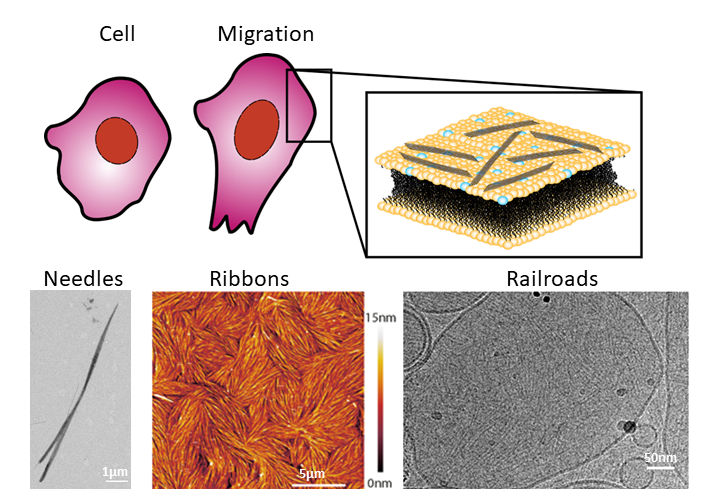
De onderzoekers bestudeerden eerst welke structuren septines van fruitvliegjes vormen bij afwezigheid van een membraan. Dit bleken dikke, rigide filamenten in de vorm van microscopisch kleine naaldjes te zijn. Vervolgens keken ze hoe septines polymeriseren in aanwezigheid van een in het lab gemaakt fosfolipidemembraan. Castro-Linares: “Tot onze verbazing zagen we dat de septines nu geen naaldjes vormden, maar netwerken van dunne filamenten, samengeklonterd in gestructureerde linten die stevig aan het membraan gebonden waren.” De onderzoekers observeerden dit door een zogenaamde atoomkrachtmicroscoop te gebruiken, een instrument dat een beeld creëert door met een zeer dunne naald een monster te scannen, ongeveer zoals iemand die braille leest. Bij het scannen van het oppervlak met de naald van de atoomkrachtmicroscoop werden de septinefilamenten over het membraan verschoven, wat bewees dat septines het membraan sterk binden en toch flexibel genoeg zijn om de vervormingen toe te laten die een celmembraan moet ondergaan.
Spoorrails
Om erachter te komen welk moleculair mechanisme de septines gebruiken om hun filamenteuze netten te vormen, maakte het team gebruik van een techniek die een nog hogere resolutie geeft: cryogene elektronenmicroscopie. Door in te zoomen op afzonderlijke filamenten ontdekten ze dat de septines eerst korte staafvormige eenheden vormen, die zich vervolgens samenvoegen tot paren van lineaire filamenten die op spoorrails lijken.
“De resultaten impliceren dat septines van fruitvliegjes in staat zijn celachtige fosfolipidemembranen te binden en een dunne netachtige structuur te vormen, als een beschermend pantser dat het celmembraan versterkt”, vat Koenderink samen. “We bestuderen nu hoe we dit nieuwe concept kunnen gebruiken om synthetische cellen te bouwen die autonoom kunnen groeien en delen met behoud van structurele integriteit.”
Dit project maakt deel uit van het grotere project 'BaSyC: Building a Synthetic Cell', waarin onderzoekers uiteindelijk cytoskeleteiwitten zullen combineren met metabolische en DNA-replicatie-mechanismen om een minimale cel te bouwen. Op Europees niveau werken onderzoekers en instituten aan hetzelfde doel met het European Synthetic Cell Initiative.
Meer informatie
Bekijk publicatie